Actualités
Présent lors de nombreux évenements et membre actif de groupes autour des dispositifs médicaux, Evamed est heureux de vous rencontrer lors de ces évenements.
Abonnez vous à la newsletter Evamed et retrouvez notre concentré d’actualité sur le secteur du dispositif médical et de la recherche clinique
Impact du MDR sur les données cliniques
Le 26 Mai 2020 était une année attendue par tous les fabricants de dispositifs médicaux, car depuis Mai 2017 (année de publication au journal officiel) le compte à rebours de l'entrée en vigueur du nouveau Règlement Européen pour les dispositifs médicaux (MDR) était lancé. Sa mise en vigueur a été retardée d'une année supplémentaire pour cause de Covid-19, soit reportée au 26 Mai 2021. Est-ce une bonne ou une mauvaise nouvelle pour tous les acteurs de la recherche clinique ? ci-dessous le calendrier prévisionnel pour la mise en application du MDR [...]
Quelques clés pour réussir son investigation clinique : sélection des sites d'investigation
La mise en place d'une investigation clinique peut répondre à plusieurs finalités telles que l'obtention de données préliminaires pour un dispositif médical innovant ou la réalisation d'un essai clinique en vue de l'obtention du marquage CE, ou du remboursement.
Comment recueillir des données cliniques rétrospectives ?
Dans cet article nos experts vous livrent quelques conseils afin de mener à bien vos recueils de données cliniques rétrospectives.
MedFIT 2019
L'évènement leader européen dédié aux partenariats d'innovation et d'investissements dans les secteurs de la technologie médicale, du diagnostic et du digital.
MEDTECH MEETUP 2019
Nous aurons le plaisir d'animer le Workshop "Calcul d'échantillon pour les études cliniques" lors du prochain MedTech Meetup. Le rendez-vous pour parler, s'informer et échanger sur l'innovation médicale. Rendez-vous le 20 Mars 2019 à Bruxelles !
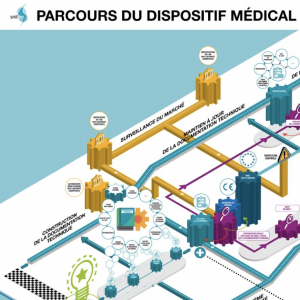
Parcours du dispositif médical avant sa commercialisation
Quel parcours suit un dispositif médical pour sa mise sur le marché ? Le SNITEM vous propose des illustrations pour comprendre toutes les étapes complexes de la mise sur le marché d'un dispositif médical.
Guide HAS pour évaluer les dispositifs médicaux connectés
La Haute Autorité de Santé (HAS) a publié un guide sur les spécificités d'évaluation clinique d'un Dispositif Médical Connecté (DMC) en vue de son accès au remboursement.
Dispositifs médicaux motorisés : une décennie de révolutions technologiques
Un article qui retrace les évolutions de ces 10 dernières années dans le domaine des Dispositifs Médicaux motorisés, au travers de plusieurs exemples d'applications significatives.
Les rendez-vous Experts MedTech
Retrouvez nos experts du dispositif médical aux Rendez-Vous Experts Medtech le mardi 12 février à Paris, pour échanger sur l'évaluation et l'investigation clinique des dispositifs médicaux.
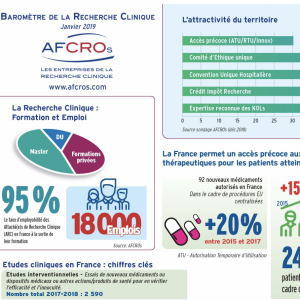
Baromètre AFCROs de la Recherche Clinique en France
L'AFCROs présente son deuxième baromètre de la Recherche Clinique en France et de ses évolutions récentes.
Vous avez un projet d'évaluation clinique
pour un dispositif médical ?